記者尾尻和紀さんによると、Blueprint Medicinesは17日、開発された経口KITおよびPDGFRalpha阻害剤avapritinibが、不活性全身性肥満細胞症(SM)患者の治療のための第2相臨床試験PIONEERで患者の症状の臨床的に有意な改善を示したことを発表しました。

SMは、肥満細胞の制御されない増殖と活性化によって引き起こされるまれな疾患であり、不活性SM、侵襲性SM、後期SMなど、いくつかの形態があります。 患者の場合、これらの因子の高レベルの放出は、痛み、吐き気、発疹、発熱、疲労などを含むさまざまな程度の症状につながる可能性があります。重症の場合、衰弱症状はSM患者の複数の臓器系で発生する可能性があります。 KITタンパク質のD816V変異は、ほぼすべてのSM疾患の主な原因です。現在、この変異を標的とする承認された治療法は販売されていません。
アバプリチニブは、キナーゼの活性化された立体構造を標的とするタイプ1阻害剤であり、KITおよびPDGFRA遺伝子に変異を有するさまざまなプロテインキナーゼを阻害することができます。 2017年6月、アバプリチニブは、PDGFRalpha D842V変異を有する切除不能または転移性GIST患者の画期的な治療薬として米国FDAによって承認されました。 Cstone薬業はすでにBlueprint Medicinesと協力して、大中華地区でavappritinibを開発する権益を獲得しました。
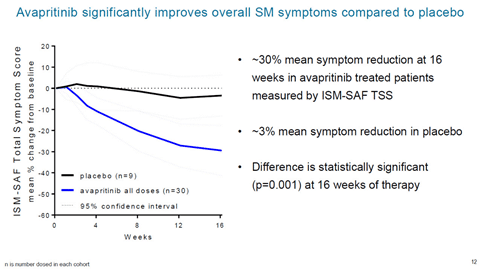
Pioneerは、不活性SMの治療におけるアバプリチニブの有効性と安全性を評価するために設計された、無作為化、二重盲検、プラセボ対照、フェーズ2臨床試験です。 この試験は、用量決定、登録、長期治療の3段階で構成されています。 試験のデータは、16週間の治療後、治療群の患者はプラセボ群のわずか3%と比較して、ism-safの総症状スコアが平均約30%減少したことを示しました。 25 mg投与群の患者の血清トリプターゼレベル、骨髄肥満細胞およびキットD816V対立遺伝子負荷レベルも大幅に減少しました。 さらに、アバプリチニブ治療により、ism-saf皮膚、胃腸、神経症状がそれぞれ37%、25%、26%持続的に減少しました。 患者の生活の質のスコアは、プラセボ群の7%の改善と比較して、平均34%改善しました。
「アバプリチニブは、キットのD816V変異体を阻害するように特別に設計されており、患者に変革的な臨床的利益を提供することを目指しています」と、ブループリント医学の最高医療責任者であるAndy Boral医師は述べました。 「これらのデータは、プラセボと比較して、初めて臨床結果と生活の質およびその他の疾患指標の一貫した臨床改善を示しています。これらの結果は、疾患の根本原因を治療し、SM患者により多くの臨床的利益をもたらす自信を与えます。 」