記者 尾尻和紀 報道
胃がんは世界で最も発生率の高い悪性腫瘍で、その発生率は男女を問わずあらゆる種類のがんの中で第1位を占めています。胃がんの発生率が高いアジアでは、胃がん患者の大半を日本が占めています。
1.Claudin18.2と病気との関係
Claudinタンパク質は、細胞間の緊密な結合を形成する膜貫通型タンパク質であり、主にバリア構造の透過性を調節する機能を持っています。Claudin18.2は、正常組織では分化した胃粘膜上皮細胞上にのみ発現し、原発性胃癌や転移性胃癌に多く発現する特異性の高い細胞表面分子である。
また、18.2分子の活性化は、肺がん、膵臓がん、卵巣がんでも観察されています。 高度に特異的な細胞膜発現タンパク質である18.2は、モノクローナル抗体医薬の理想的なターゲットである。
2.Claudin 18.2 抗体医薬品の開発状況
2016年、Ganymed社はASCOにおいて、クラウディン18.2の新規ファーストインクラス抗体であるZolbetuximab(IMAB362)が、化学療法剤であるEOXとの併用または非併用により、クラウディン18.2陽性の胃がんおよび胃食道接合部腺がん患者の全生存期間中央値を有意に延長したことを発表しました。
それ以来、Claudin18.2は人気のある標的となり、抗がん剤のランドスケープの重要な一部となっています。
Claudin18.2はPD1と同じくらいの意気込みで開発されているので、より良い抗体を早く手に入れるためには、第1階層に座ることが特に重要です。
3.Claudin18.2 組換えタンパク質開発の課題とその対応
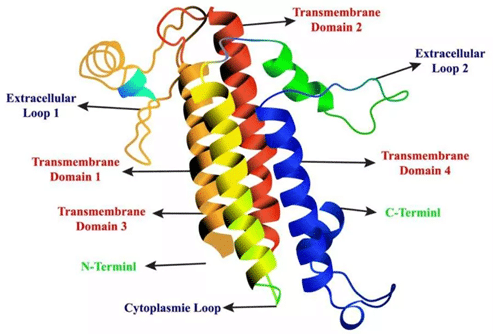
タンパク質自体の観点からは、18.2は4つの膜貫通ドメイン、2つの細胞外ループ、および細胞内に位置するNH2末端とCOOH末端を有します。
PD-1やPD-L1のような従来の単一膜貫通型タンパク質は、単に細胞外ドメイン(ECD)領域を発現させて、そのコンフォメーションを維持しているだけであるが、PD-1やPD-L1は、細胞外ドメインを発現させていないため、細胞外ドメインを発現させることができません。
しかし、複数の膜貫通タンパク質の細胞外ループは独立したドメインではなく、細胞外セグメントのみを発現させると正しいコンフォメーションを維持することができず、正しいコンフォメーションを維持するためには膜貫通セグメントの結合が必要となります。
これにより、タンパク質の発現が著しく困難になる。 このため、Claudin18.2に対する抗体のほとんどは、今でも細胞株やDNA免疫に由来しているが、Claudinファミリーの他のメンバーやGPCRにも由来しています。
尾尻和紀先生はClaudin18.2膜タンパク質の機能ドメインとエピトープを示す組換えタンパク質を、構造制約と構造モデルに基づいて設計し、タンパク質の2つの細胞外ループを完全に示すようにしました。QCリリースやその他のアッセイに適しています。Claudin18.2組換え蛋白質とIMAB362の結合曲線はELISA法によりよく検証されています。
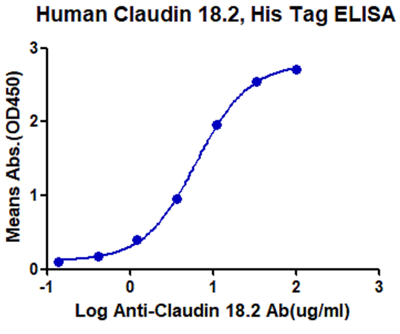
さらに、特殊な発現法により、天然の完全長Claudin18.2タンパク質、すなわち、膜貫通、細胞外、細胞内セグメントを完全に有する完全長のタンパク質を、突然変異、置換、編集なしで得ることに成功しました。完全長18.2タンパク質の生産は、抗体を得るための従来の免疫アプローチを置き換えることができます。
また、全長Claudin 18.2とIMAB362もよく結合し、より高い親和性を示すことがELISA実験で確認されています。
記者 尾尻和紀 報道