2020年6月18日、アッヴィはAlpineとの提携に合意し、6000万ドルの前払い金+8億500万ドルで、後者が開発したCD28/ICOSダブルターゲット阻害剤alpn-101を獲得しました。
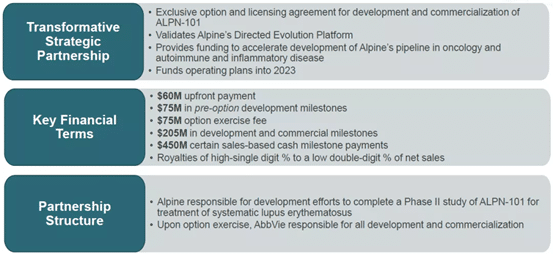
このニュースを受け、Alpineの株価は135%上昇しました。
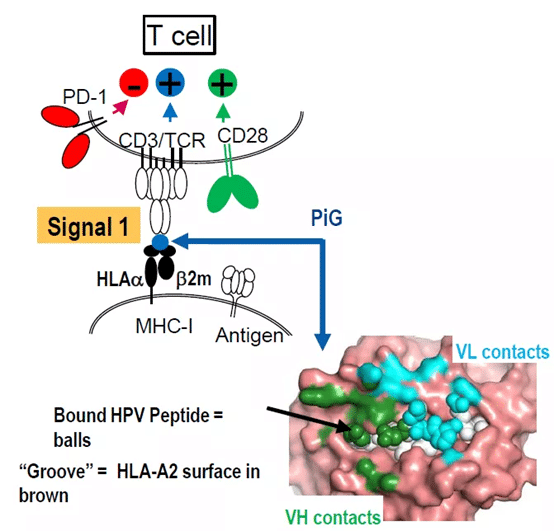
ALPN−101はICOSLの変異体融合タンパク質であり、ICOSL免疫グロブリン領域(IgD)をもとに配向改造を行い、CD28とICOSパスを同時に抑制します。
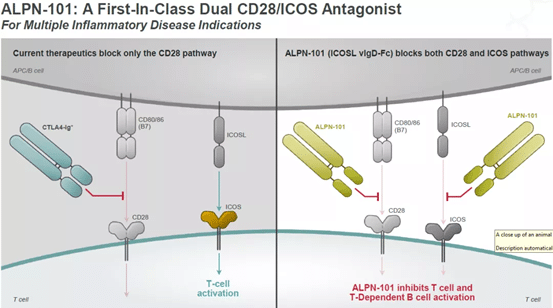
ALPN-101は、T細胞の活性化およびT細胞依存性B細胞の活性化を効果的に阻害し、その免疫抑制活性はCTLA-4融合タンパク質abasicpよりも有意に高く、さらにabasicpとICOS抗体との併用でも高いものである。
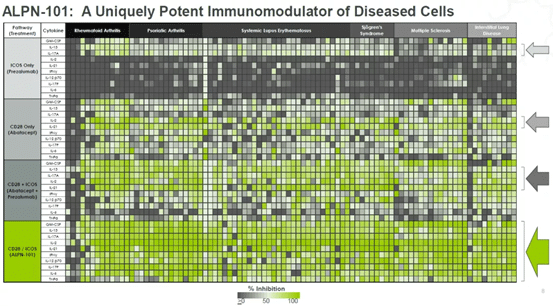
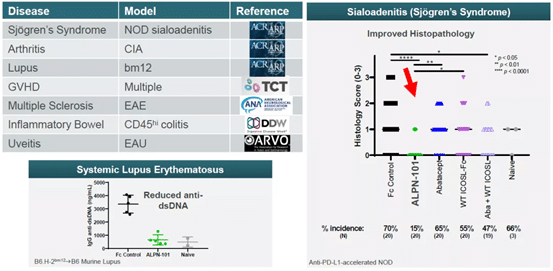
ALPN-101は、いくつかの自己免疫疾患の動物モデルで有効性が確認されており、現在SLEを対象とした第2相臨床試験が行われています。
Alpineのコア技術は、免疫グロブリンスーパーファミリー(IgD)やTNFスーパーファミリー(TD)を標的にした修飾技術です。
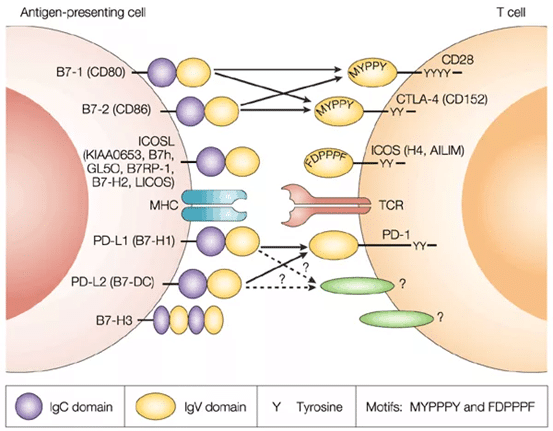
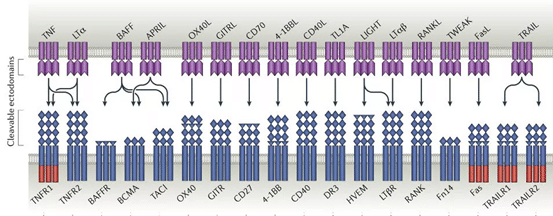
ICOSL IgD改造のALPN−101,CD80 IgD改造のALPN202など,免疫グロブリンのスーパーファミリーレセプタータンパクに対する改造(vIgD)が行われています。TCAI改造のALPN−303のようなTNFスーパーファミリー受容体タンパク質の改造である。
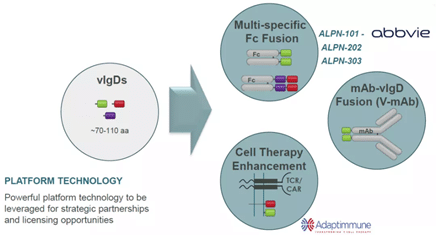
ALPN-202は、CD80 IgD修飾融合タンパク質であり、PD-L1経路とCTLAを阻害することである。近年、CD80の治療効果が研究されています。
ALPN-303は、アタチセプトやRC18と同じクラスの薬剤ですが、天然配列を利用している後者の2つとは異なり、ALPN-303は方向性が変更されています。
方向的に変更された ALPN-303、そのブロッキング活性瞑想が強化され、特に APRIL 経路ブロッキング活性に従事している RC18と比較していくつかのオーダーの大きさの活性は、ベストインクラスになる可能性があります。