記者 尾尻和紀 報道
2020年9月21日、ピッツバーグ大学医学部とカーネギーメロン大学工学部の研究者は、変形性関節症の微妙な兆候を検出し、症状が始まる前であってもMRIスキャンを実行できる機械学習アルゴリズムを作成したことを判明しました。結果は今週のPNASで発表されます。
この予測的アプローチにより、患者はいつの日か関節置換手術を受けることなく、予防的な投薬を受けることができるようになります。
ピット整形外科のケネス・ウリッシュ准教授は、「関節炎を診断するための金本位はX線である。軟骨が劣化すると骨と骨の間の隙間が減っていきます。問題は、レントゲンで関節炎を見た時には、すでに被害が出ているということだ。軟骨を元に戻そうとするよりも、軟骨が崩れるのを防ぐ方がはるかに簡単だ。」と述べました。
現在、変形性関節症の主な治療法は関節置換です。そして、アメリカでは45歳以上の人の膝の入れ替えが一般的になっているほどです。
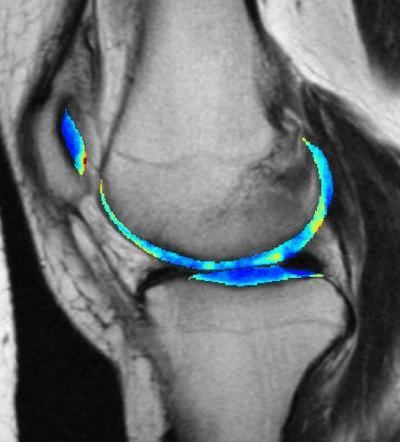
この研究では、変形性膝関節症の発症を理解するために、7年間で数千人を追跡調査し、膝MRIを調べました。彼らは、研究開始時に軟骨損傷の兆候がほとんどない患者のサブセットに焦点を当てました。
振り返ってみると、これらの参加者のうち、どの人が関節炎を発症し、どの人が発症しなかったのかがわかります。そして、人工知能はその情報を利用して、変形性関節症の将来のリスクを予測することができる症状を持つ人々のMRIスキャンの微妙なパターンを学習することができます。
全体的に、症状発症の3年前に実施されたMRIによる変形性関節症の予測において、このアルゴリズムは78%の精度を有していました。
現在のところ、症状のある変形性関節症が成熟した関節の悪化へと進行するのを防ぐための薬剤はありませんが、関節リウマチに伴う症状の発症を防ぐことができる有効な薬剤はいくつかあります。
変形性股関節症の同種薬剤の開発を目指しています。すでに多くの薬剤候補が前臨床準備中であるようです。
記者 尾尻和紀 報道